Rumus Hukum Henry. Ln P1P2 ΔHuapR 1T2 - 1T1.

Belajar Matematika Simpel Pintar Pelajaran Tetapan Kesetimbangan Pada Tekanan Parsial Gas Kp Pola Soal Pembahasan Kimia
Tetapan Kesetimbangan pada Tekanan Parsial Gas K p Contoh Soal Pembahasan Kimia - Tetapan kesetimbangan berdasarkan tekanan gas dinyatakan dengan notasi K p yaitu hasil kali tekanan parsial gas-gas hasil reaksi dibagi dengan hasil kali tekanan parsial gas-gas pereaksi masing-masing tekanan parsial gas dipangkatkan koefisiennya menurut persamaan reaksi.

Rumus mencari tekanan parsial. Untuk sistem kesetimbangan gas perhitungan tetapan kesetimbangan gas Kp menggunakan tekanan parsial masing - masing gas. 2KClO₃ s 2KCl s 3O₂ g Gas oksigen dapat dikumpulkan di atas permukaan air seperti yang ditunjukkan pada Gambar 515. Jadi tetapan kesetimbangan Kp adalah 0787.
M A g n B g p C g q D g Maka rumus Kp sebagai berikut. Jika diketahui tekanan total suatu reaksi gas maka tekanan parsial tiap-tiap zatnya dapat ditentukan. Jumlah mol total saat reaksi gas mencapai kesetimbangan dapat dicari dengan rumus gas ideal.
Pada industri pembuatan asam sulfat gas SO3 mengalami dekomposisi menjadi SO2 dan O2 memebentuk reaksi kesetimbangan berikut. Misalnya jika potasium klorat KClO₃ dipanaskan akan terurai menjadi KCl dan O₂. Rumus Kpnya ternyata sama dengan rumus jumlah tekanan total.
Kp 32 x 10 2 0082 x 300 1. Kita dapat lihat bahwa tekanan total pada reaksi diatas sama dengan jumlah tekanan parsial NH3 dan HCl saja karena wujud dari NH4Cl adalah s sehingga tidak punya tekanan. Hubungan Kc dan Kp.
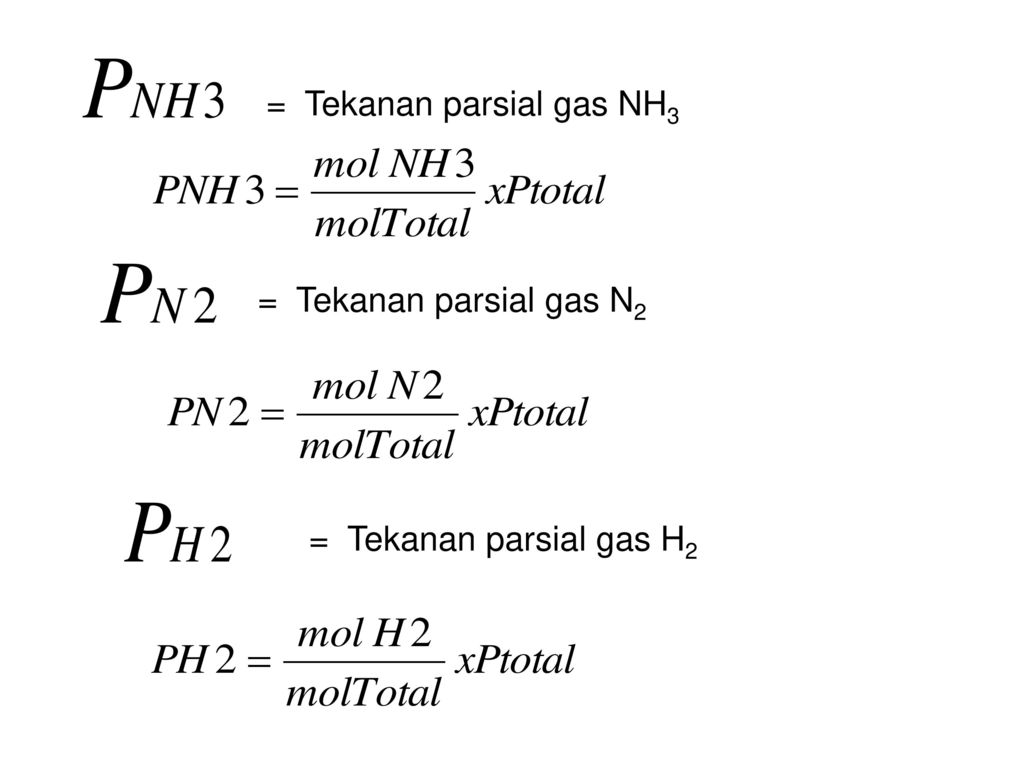
Rumus Menghitung Tetapan Kesetimbangan Tekanan Parsial Gas Kp Tetapan kesetimbagan tekanan parsial gas dapat dirumuskan dengan persamaan seperti berikut. Rumus Tekanan Ilmu Fisaka Yang Berhubungan Dengan Rumus Tekanan Besaran Gaya. Rumus tekanan parsial masing - masing zat dalam kesetimbangan.
Karena tekanan parsial tiap gas telah diketahui maka untuk mencari harga Kp nya kita bisa gunakan rumus berikut. P tekanan atm V. Konstanta Henry dinyatakan sebagai.
Rumus hukum Henry menetapkan hubungan antara tekanan parsial dari gas murni dan fraksi molnya dalam pelarut. Al x P2 A2 x P2 A jumlah gas yang larut P tekanan parsial gas pada permukaan cairan Hukum ini penting untuk menjelaskan tentang turunnya tekanan oksigen atau berkurangnya persediaan oksigen bila isi tetap maka tekanan gas tersebut Hukum. Tetapan kesetimbangan parsial gas atau Kp adalah hasil kali tekanan parsial gas-gas hasil reaksi dibagi dengan hasil kali tekanan parsial gas-gas pereaksi masing-masing tekanan parsial gas dipangkatkan koefisiennya menurut persamaan reaksi.
Kp 32 x 10 2 0082 x 300 1. Perhitungan Kp hanya untuk zat yang fasanya gas. Anda akan melihat perbedaan kecil dalam nilainya dengan mencari tekanan parsial terlebih dahulu lalu tekanan total dan mencari tekanan total terlebih dahulu kemudian tekanan parsial.
Sedangkan dari sudut pandang jenis nya gaya juga. PV nRT di mana P adalah tekanan V adalah volume n adalah jumlah mol R adalah konstanta gas dan T adalah suhu. Hukum tekanan parsial Dalton berguna untuk menghitung volume gas yang dikumpulkan di atas permukaan air.
Besaran Gaya adalah segala bentuk interaksi yang dapat menyebabkan sebuah benda mengalami perubahan gerak dari berbagai sisi yang dinilai dari arah nya gaya merupakan besaran vektor fisika karena gaya memiliki nilai dan arah tertentu. Ingatlah bahwa nilai yang diberikan disajikan sebagai nilai perkiraan karena pembulatan ke satu atau dua tempat desimal untuk membuat nilai lebih mudah dipahami. Contoh Soal Perhitungan Penambanhan Jumlah Mol Pada Reaksi Setimbanga.
Adalah konstanta volatilitas khusus untuk gas yang diberikan. Rumus Menghitung Tetapan Kesetimbangan Tekanan Parsial Gas Kp Tetapan kesetimbagan tekanan parsial gas dapat dirumuskan dengan persamaan seperti berikut. Dalam kimia tekanan uap adalah tekanan yang diberikan dinding wadah yang tertutup saat zat kimia di dalamnya menguap berubah menjadi gas.
Untuk mencari tekanan uap pada suhu yang diketahui gunakan persamaan Clausius-Clapeyron. Kp Kc RT Δn. Kp Kc RT Δn.
Sedangkan rumus Kp nya adalah Kp PNH3 x PHCl0. Jadi tetapan kesetimbangan Kp adalah 0787. Hukum ini mengukur kelarutan gas dalam pelarut cair dengan mana gas berada dalam kontak.
Karena zat yang berfasa padat dan cair tidak mempengaruhi tekanan. Hukum yang digunakan untuk mencari tekanan parsial mengasumsikan suhu sistem konstan dan gas berperilaku sebagai gas ideal mengikuti hukum gas ideal. Tekanan Parsial Gas Kesetimbangan Kimia Dalam tulisan ini kita akan mempelajari pengertian kesetimbangan kimia contoh aplikasi kesetimbangan kimia dalam industri menentukan dan menghitung besarnya konstanta kesetimbangan kimia mempelajari berbagai jenis kesetimbangan kimia memanipulasi persamaan kesetimbangan kimia serta mengkaji faktor-faktor yang dapat menggeser.
Contoh Soal Perhitungan Penambanhan Jumlah Mol Pada Reaksi Setimbanga.

Kesetimbangan Kimia Pengertian Faktor Hukum Rumus Contoh

Tekanan Parsial Co2 Pada Keadaan Setimbang Adalah A 0 05 Atmb 0 075 Atmc 0 1 Atmd 0 025 Atme Brainly Co Id

Kesetimbangan Kimia Pengertian Rumus Soal

Penentuan Tetapan Kesetimbangan

Persamaan Laju Reaksi Penjelasan Rumus Contoh Soal Dan Jawaban

Kesetimbangan Menentukan Tekanan Parsial Kimia Sma Youtube
Hukum Tetapan Kesetimbangan Konsentrasi Ppt Download

Hukum Dalton Isi Penerapan Rumus Dan Contoh Soal Materiipa Com



Comments
Post a Comment